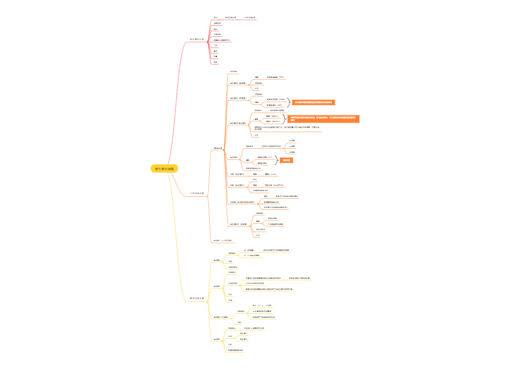
生物体内发生的各种氧化反应的统称
反应的本质都是脱氢、失电子或加氧
被氧化的物质相同,终产物和释放的能量也相同
生物氧化的主要方式是脱氢
条件比较温和
生物氧化是在一系列酶、辅酶(辅基)和电子传递体的作用下逐步进行的,每一步释放一部分能量
可以防止能量的骤然释放而损害有机体
可以让机体更好地捕获能量合成ATP
方便了机体对其进行调控
由一系列电子传递体构成的链状复合体
又称电子传递系统(ETS)
主要差别在于最终的电子受体
下面主要介绍需氧生物
NADH呼吸链
FADH2呼吸链
通过与氧化磷酸化的偶联产生ATP
异柠檬酸脱氢酶
α-酮戊二酸脱氢酶
苹果酸脱氢酶
在上述脱氢酶的催化下,各种底物将电子和氢交给氧化型NAD+
NAD+得到氢和电子后被还原为NADH/H+
NADH离开酶的活性中心,扩散到呼吸链的“入口”,留下氢和电子后离开呼吸链去再次与脱氢酶结合
作为一种流动的电子传递体
是呼吸链上以NADH为底物的脱氢酶
直接从其他脱氢酶催化产生的NADH中获得电子,将电子交给其他的电子传递体
与酶活性中心紧密结合,一般不会离开,防止对其他分子的破坏
将琥珀酸氧化成延胡索酸
留住琥珀酸在氧化时释放的电子,使其先被辅基FAD捕获,再转移给其他的电子传递体
产生的FADH2是呼吸链的又一重要电子供体
又名泛醌(UQ)
哺乳动物的辅酶Q常称Q10
一次可传递两个电子,也可传递一个
作为流动的电子传递体
又称铁硫中心或铁硫簇
Fe和S通过配位键结合
通过Fe的价态变化传递电子
通过血红素铁的价态变化传递电子
a
b
充当流动的电子传递体
所有有氧生物呼吸链的末端电子受体
1*O2+4*e-=2*O2-
表示一种物质的氧化还原能力
值越小,还原型越强,越容易失去电子被氧化
呼吸链中各种组分的排列顺序应当由低E0'依次向高E0'排列
各传递体在体外测得E0'与内膜环境的实际值可能有出入,实验结果仅供参考
确定在有氧环境下氧化反应达到平衡时各电子传递体的还原程度
从呼吸链的起点到终端,各组分的还原程度一定是递减的
被阻断部位的上游,各个传递体应为还原型,下游应为氧化型
可以插入到呼吸链特定的部位,接受E0'值比它低的传递体上的电子
分析不同的抑制剂和不同的人工电子受体作用呼吸链的结果
差速离心获得线粒体
毛地黄干处理除去外膜
渗透压冲击获得碎片
去垢剂增溶,离子交换层析简单分离呼吸链
NADH→CoQ
琥珀酸→CoQ
CoQ→Cyt c
Cyt c→O2
ATP合酶
NADH→复合体I→CoQ→复合体III→Cyt c→复合体IV→O2
琥珀酸→复合体II→CoQ→复合体III→Cyt c→复合体IV→O2
既含蛋白质,又含辅因子
构成蛋白质的亚基有的是核基因组编码的,有的是线粒体基因组编码的
催化NADH的氧化和CoQ的还原
以NADH为底物,FMN和铁硫蛋白为辅基
NADH→FMN→铁硫蛋白→CoQ
2*e-→4*H+泵出线粒体基质
催化琥珀酸的氧化和CoQ的还原
只接受来自琥珀酸的氢和电子
与TCA中的琥珀酸脱氢酶是同一种酶
铁硫蛋白
细胞色素b560
琥珀酸→FAD→铁硫蛋白→细胞色素b560→CoQ
无H+泵出
磷酸甘油脱氢酶和脂酰-CoA脱氢酶也能产生FADH2,但不通过复合体II进入呼吸链
催化CoQH2的氧化和细胞色素c的还原
细胞色素b
细胞色素c1
铁硫蛋白
在线粒体内膜上通常形成二聚体
CoQH2→细胞色素b→铁硫蛋白→细胞色素c1→细胞色素c
2*e-→4*H+泵出
催化细胞色素c的氧化和O2的还原
血红素a
血红素a3
2*CuA
1*CuB
细菌只有3-4个
最大的多肽
与血红素a和a3结合
参与电子从血红素a到O2的传递
通过Cys与两个CuA结合
参与还原型细胞色素c的结合
细胞色素c→CuA→血红素a→a3CuB双核中心→O2
2*e-→2*H+泵出
不产生跨膜质子梯度
对鱼藤酮不敏感
不产生跨膜质子梯度
对KCN不敏感
没有Cu,但有双铁氧化中心
具有完整呼吸活性的呼吸链超复合体
I1 III2 IV1
与电子传递相偶联的合成ATP的方式
用底物磷酸化的基质解释氧化磷酸化
电子传递中释放的能量变成了一种含高能键的中间物,将来交给ADP
电子在呼吸链上传递的过程中导致某些蛋白质从低能构象变为高能构象,当这些蛋白质从高能构象恢复到低能构象时,ATP被合成
电子在沿呼吸链向下游传递的时候,释放的自由能先转化为跨线粒体内膜或跨细菌和古菌质膜的质子梯度,随后质子梯度中蕴藏的电化学势能被直接用来驱动ATP的合成
质子多的一侧(正电荷多)
质子少的一侧(负电荷多)
驱动ATP合成的质子梯度
氧化磷酸化的进行需要完整的线粒体内膜的存在
使用精确的pH计可以检测到跨线粒体内膜两侧质子梯度的存在
破坏质子驱动力的化学试剂能够抑制ATP的合成
从线粒体纯化得到的一种酶,能够直接利用质子梯度合成ATP
称为F1Fo-ATP合酶
人工建立的跨线粒体内膜的质子梯度也可驱动ATP的合成
亚基I上的带电荷氨基酸残基构成通道,让质子通过
通常4*H+→1*ATP合成
2e-→10H+→2.5ATP
2e-→6H+→1.5ATP
呈球状,为可溶性
3*α亚基
3*β亚基
形成中央柄
在质子流驱动下不断转动,影响β亚基的构象
1*δ亚基
1*ε亚基
直接与ATP的合成和释放相关
呈柄状,横跨线粒体内膜
1*a亚基
2*b亚基
组成一个C单位
构成桶装的被动质子通道
利用质子驱动力驱动ATP的合成和释放
F型质子泵
在活性中心合成ATP并不需要质子驱动力,与活性中心结合的ATP或ADP处于平衡
正常条件下ATP水解的ΔG为较大负值
在H2O浓度极低时ATP合成为较小负值
如果没有质子流过Fo,与活性中心结合的ATP就不会与酶解离
3个β亚基因为与γ亚基的不同部位结合,所以采取不同构象
松散构象
开放构象
紧密构象
处于T态的β亚基紧密结合1分子ATP,ATP与ADP+Pi处于平衡,但ATP并不能与它解离;处于L态的β亚基结合ADP和Pi,但并不能释放核苷酸;处于O态的β亚基能够释放结合的核苷酸
3种状态的β亚基可以相互转变,转变过程由γ亚基的转动所驱动
γ亚基的动力来自质子通过Fo的流动
每消耗3H+,γ亚基转动120°,其中一个β亚基合成并释放一个ATP
将ATP转运出线粒体消耗1*H+
质子是通过与各c亚基上的酸性AA(Asp或Glu)可逆结合和解离而传递的
大多数生物是Glu,少数是Asp
在c亚基第二段跨膜α螺旋的中间位置
a亚基的一个跨膜α螺旋的最后一个AA——Arg210
一个面向膜间隙,充当质子的进口
一个面向基质,充当质子的出口
ATP和H2O18混合时,出现的Pi四个O都是O18
F1的晶体结构数据
基因工程改造过的F1的转动研究数据
一些抑制剂的作用
在体内存在抑制因子1(IF1),抑制在质子驱动力低迷时ATP的水解
抑制呼吸链上的电子传递
抗霉素A、鱼藤酮
作用复合体IV的Fe,占用O2与其结合的配位键
抑制质子通过
寡霉素、DCCD
将贮存在质子梯度之中的电化学势能全部转变成了热能
可使细胞内脂肪和碳水化合物等物质的生物氧化更加旺盛
通常为脂溶性的质子载体
2, 4-二硝基苯酚(2, 4-DNP)
在线粒体内膜上形成质子通道
又名产热素
主要存在于动物的褐色脂肪组织(BAT)
与机体的非颤抖性产热有关
防止线粒体膜电位过高而形成太多活性氧(ROS)
1*H+→1*ATP转运出线粒体
苍术苷
米酵菌酸
在电子传递过程中,每消耗1mol氧原子所消耗的无机磷酸的物质的量
P/O值越高,氧化磷酸化的效率越高
NADH呼吸链的P/O值为2.5
FADH2呼吸链的P/O值为1.5
由ADP浓度控制氧化磷酸化
F1Fo-ATP合酶活性↑
质子浓度↓
电子传递速率↑
耗氧率↑
细胞呼吸↑